Що таке барію сульфат? Як одержують сульфат барію?
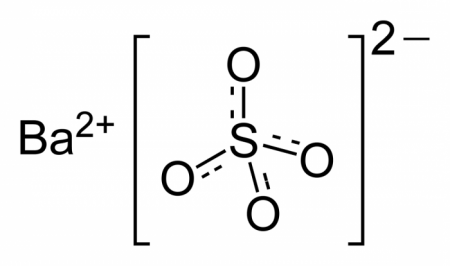
Барію сульфат – це неорганічне речовина з хімічною формулою BaSO 4 . Являє собою білий порошок без запаху, нерозчинний у воді. Його білизна і непрозорість, а також висока щільність визначають основні області застосування.
Вперше він був виявлений шведськими хіміками Шеєле і Ганом у 1774 році в складі так званого важкого шпату. Звідси виникло і назва мінералу (від грец. «барис» – важкий), а потім і самого металу, коли в 1808 р. його виділив у чистому вигляді Гемфрі Деві. Яка маса сульфату барію? Молярна маса його дорівнює 23343 г/моль. Він володіє надзвичайно високою питомою вагою – від 425450 г/см 3 . З огляду на нерозчинність у воді, висока щільність робить його незамінним в якості наповнювача водних бурових розчинів.
Яка маса сульфату барію? Молярна маса його дорівнює 23343 г/моль. Він володіє надзвичайно високою питомою вагою – від 425450 г/см 3 . З огляду на нерозчинність у воді, висока щільність робить його незамінним в якості наповнювача водних бурових розчинів.
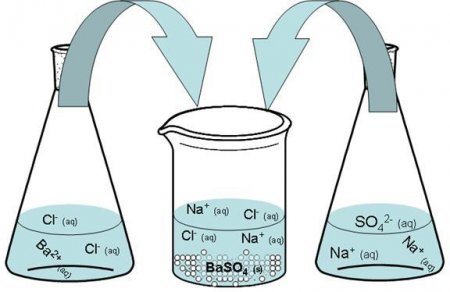
Візьмемо також водний розчин хлориду барію – BaCl 2 , молекула якого розділені на три іона: один Ba 2+ і два Cl - . BaCl 2 -> Ba 2+ + 2Cl - Змішаємо водний розчин сульфату і суміш, що містить хлорид. Барію сульфат утворюється в результаті з'єднання в одну молекулу двох іонів з однаковим по величиною та протилежним за знаком зарядом. Ba 2+ + SO 4 2 - -> BaSO 4 Нижче ви можете побачити повне рівняння цієї реакції (так зване молекулярне). Na 2 SO 4 + BaCl 2 -> 2NaCl + BaSO 4
В результаті утворюється нерозчинний осад сульфату барію.
Термін "первинний" барит відноситься до товарної продукції, яка включає в себе сирий матеріал (отримується з шахт і кар'єрів), а також продукти простого збагачення такими методами, як промивка, осадження, сепарація у важких середовищах, флотація. Велика частина сирого бариту вимагає доведення його до мінімальної чистоти і щільності. Мінерал, який використовується в якості наповнювача, подрібнюють і просівають до однорідного розміру так, щоб, щонайменше, 97 % його частинок мали розмір до 75 мкм, і не більше 30 % були менше 6 мкм. Первинний барит також повинен бути досить щільним, щоб його питома вага склала 42 г/см 3 або вище, але при цьому досить м'яким, щоб не пошкодити підшипники.
Історія назви
Барій відноситься до щелочноземельним металів. Останні названі так тому, що, за словами Д. І. Менделєєва, їх сполуки утворюють нерозчинну масу землі, а оксиди "мають землистий вид". Барій у природі міститься у вигляді мінералу бариту, який представляє собою барію сульфат з різними домішками.Вперше він був виявлений шведськими хіміками Шеєле і Ганом у 1774 році в складі так званого важкого шпату. Звідси виникло і назва мінералу (від грец. «барис» – важкий), а потім і самого металу, коли в 1808 р. його виділив у чистому вигляді Гемфрі Деві.
Фізичні властивості
Оскільки BaSO 4 – це сіль сірчаної кислоти, то її фізичні властивості почасти визначаються самим металом, який є м'яким, хімічно активним і сріблясто-білим. Природний барит безбарвний (іноді білий) і прозорий. Хімічно чистий BaSO 4 має колір від білого до блідо-жовтого, він негорючий, з температурою плавлення 1580°С.
Хімічні властивості
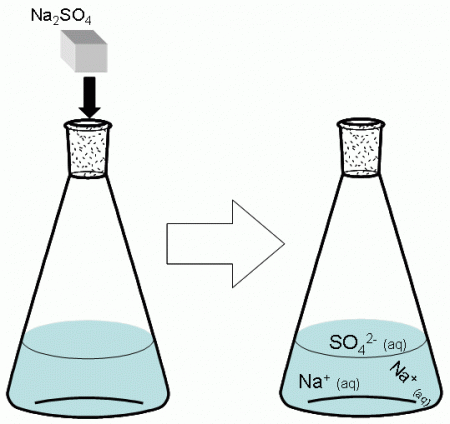
BaSO 4 – це одне з найбільш важкорозчинних в воді сполук. Його можна отримати з двох добре розчинних солей. Візьмемо водний розчин натрію сульфату – Na 2 SO 4 . Його молекула у воді дисоціюють на три іона: два Na + і один SO 4 2 - . Na 2 SO 4 -> 2Na + + SO 4 2 -Візьмемо також водний розчин хлориду барію – BaCl 2 , молекула якого розділені на три іона: один Ba 2+ і два Cl - . BaCl 2 -> Ba 2+ + 2Cl - Змішаємо водний розчин сульфату і суміш, що містить хлорид. Барію сульфат утворюється в результаті з'єднання в одну молекулу двох іонів з однаковим по величиною та протилежним за знаком зарядом. Ba 2+ + SO 4 2 - -> BaSO 4 Нижче ви можете побачити повне рівняння цієї реакції (так зване молекулярне). Na 2 SO 4 + BaCl 2 -> 2NaCl + BaSO 4
В результаті утворюється нерозчинний осад сульфату барію.
Товарний барит
На практиці вихідною сировиною для одержання товарного сульфату барію, призначеного для використання в бурових розчинах при бурінні нафтогазових свердловин, є, як правило, мінеральний барит.Термін "первинний" барит відноситься до товарної продукції, яка включає в себе сирий матеріал (отримується з шахт і кар'єрів), а також продукти простого збагачення такими методами, як промивка, осадження, сепарація у важких середовищах, флотація. Велика частина сирого бариту вимагає доведення його до мінімальної чистоти і щільності. Мінерал, який використовується в якості наповнювача, подрібнюють і просівають до однорідного розміру так, щоб, щонайменше, 97 % його частинок мали розмір до 75 мкм, і не більше 30 % були менше 6 мкм. Первинний барит також повинен бути досить щільним, щоб його питома вага склала 42 г/см 3 або вище, але при цьому досить м'яким, щоб не пошкодити підшипники.
Одержання хімічно чистого продукту
Мінеральний барит часто забруднений різними домішками, в основному, оксидами заліза, ми, офарблюють його в різні кольори. Він обробляється карботермическим способом (нагріванням з коксом). В результаті утворюється сульфід барію. BaSO 4 + 4 С -> BaS + 4 З Останній, на відміну від сульфату, розчинний у воді і легко реагує з киснем, галогенами та кислотами. BaS + Н 2 SO 4 -> BaSO 4 + Н 2 S Щоб отримати високочистий вихідний продукт, використовується сірчана кислота. Сульфат барію, утворений за такого процесу, часто називають бланфиксом, що в перекладі з французької означає "білий фіксований". Він часто зустрічається в споживчих продуктах, таких як фарби. В лабораторних умовах сульфат барію утворюється шляхом об'єднання в розчині іонів барію і сульфат-іонів (см. вище). Оскільки сульфат є найменш токсичною сіллю барію з-за її нерозчинності, відходи, що містять інші його солі, іноді обробляють сульфатом натрію, щоб зв'язати весь барій, є достатньо токсичним.З сульфату в гідроксид і назад
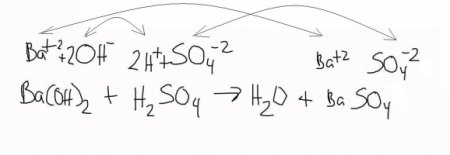
Історично барит використовувався для виробництва гідроксиду барію Ba(OH) 2 , необхідного при рафінуванні цукру. Це взагалі дуже цікаве і широко використовується в промисловості з'єднання. Воно добре розчинно у воді, утворює розчин, відомий як баритовая вода. Її зручно використовувати для зв'язування сульфат-іонів у різних складах шляхом утворення нерозчинного BaSO 4 . Вище ми бачили, що при нагріванні в присутності коксу з сульфату легко отримати водорозчинний сульфід барію – BaS. Останній же при взаємодії з гарячою водою утворює гідроксид. BaS + 2H 2 O -> Ba(OH) 2 + H 2 S^ Гідроксид барію та сульфату натрію, взяті в розчинах, при змішуванні дадуть нерозчинний осад сульфату барію і їдкий натрій. Ba(OH) 2 + Na 2 SO 4 = BaSO 4 + 2NaOH Виходить, що природний барію сульфат (барит) промисловим способом спочатку перетворюється на гідроксид барію, а потім служить для отримання того ж сульфату при очищенні різних сольових систем від сульфат-іонів. Точно так само буде проходити реакція і при очищенні від іонів SO 4 2 - розчину сірчанокислої міді. Якщо зробити суміш "гідроксид барію + сульфат міді", то в результаті вийде гідроксид міді і нерозчинний барієвий сульфат. CuSO 4 + Ba(OH) 2 -> Cu(OH) 2 + BaSO 4 V Навіть в реакції з самої сірчаною кислотою її сульфат-іони будуть повністю пов'язані барієм.Використання в бурових розчинах
Близько 80 % світового виробництва сульфату барію, очищеного і подрібненого бариту, споживається в якості компонента бурових розчинів при створенні нафтогазових свердловин. Добавка його збільшує щільність рідини, закачиваемой в свердловину, з метою кращого опору високого пластового тиску і запобігання проривів. Коли свердловина буриться, долото проходить через різні утворення, кожне з яких має свої характеристики. Чим більше глибина, тим більший відсоток бариту повинен бути присутнім в структурі розчину. Додатковою перевагою є те, що барію сульфат – немагнитное речовина, тому він не заважає проведенню різних вимірювань у свердловині за допомогою електронних пристроїв.Лакофарбова і паперова промисловість
Велика частина синтетичного BaSO 4 використовується в якості компонента білого пігменту для фарб. Так, бланфикс в суміші з двоокисом титану (TiO 2 ) продається в якості білої олійної фарби, застосовуваної в живопису. Поєднання BaSO 4 і ZnS (сульфід цинку) дає неорганічний пігмент, який називається литопоном. Він використовується в якості покриття для певних сортів фотопаперу. Зовсім недавно барію сульфат був застосований для освітлення паперу, призначеного для струменевих принтерів.Застосування в хімічній промисловості та кольоровій металургії
У виробництві поліпропілену та полістиролу BaSO 4 використовують в якості наповнювача в пропорції до 70 %. Він має ефект збільшення стійкості пластмас до дії кислот і лугів, а також надає їм непрозорість. Він також використовується для виробництва інших сполук барію, зокрема його карбонату, який застосовується для виготовлення світлодіодного скла для телевізійних і комп'ютерних екранів (історично в електронно-променевих трубках). Форми, використовувані в відливання металів, часто покривають барію сульфатом для запобігання зчеплення з розплавленим металом. Так поступають при виготовленні анодних мідних пластин. Їх відливають у мідні виливниці, покриті шаром сульфату барію. Коли рідка мідь твердне у вигляді готової анодної пластини, вона може бути легко вилучена з ливарної форми.Піротехнічні пристрої
Оскільки сполуки барію випускають зелений світло при горінні, то солі цієї речовини часто використовуються піротехнічних формулах. Хоча нітрат і хлорат є більш поширеними, ніж сульфат, останній широко використовується в якості компонента піротехнічних стробоскопів.Рентгеноконтрастний препарат
Барію сульфат є рентгеноконтрастні агентом, використовуваним для діагностики певних медичних проблем. Так як подібні речовини є непрозорими для рентгенівських променів (блокують їх внаслідок своєї високої щільності), області тіла, в яких вони локалізуються, з'являються білі ділянки на рентгенівській плівці. Це створює необхідне відмінність між одним (діагностуються) органом та іншими оточуючими його) тканинами. Контраст допоможе лікарю побачити будь-які особливі умови, які можуть існувати в цьому органі або частини тіла. Барію сульфат приймається через рот або ректально за допомогою клізми. У першому випадку він робить стравохід, шлунок або тонкий кишечник непрозорим для рентгенівських променів. Таким чином, вони можуть бути сфотографовані. Якщо речовина введено за допомогою клізми, то товсту кишку або кишечник можна побачити і зафіксувати рентгенівськими променями. Доза сульфату барію буде різною для різних пацієнтів, все залежить від типу тесту. Препарат випускається у вигляді спеціальної медичної барієвої суспензії або в таблетках. Різні тести, при яких потрібен контраст і рентгенівське обладнання, вимагають різної кількості суспензії (в деяких випадках необхідний прийом препарату у формі таблетки). Контрастна речовина має використовуватися лише під безпосереднім контролем лікаря.Схожі добрі поради по темі

Сульфат амонію: формула, склад, одержання і застосування
Сульфат амонію — речовина, яка може бути отримана в результаті здійснення деяких хімічних реакцій. Використовується в різних сферах народного

Металевий блиск сірки: чи існує? Фізичні та хімічні властивості сірки
Блиск – це здатність речовини відбивати промені світла. Це властивість перебуває у безпосередній залежності від специфіки хімічних зв'язків в

Що таке сіль? Формула, властивості солі (хімія)
Для того щоб відповісти на питання, що таке сіль, зазвичай довго замислюватися не доводиться. Це хімічна сполука у повсякденному житті зустрічається

Прикольні запитання для дівчат, з якими хочеться завести знайомство
Часто задається і давно приївся питання від хлопця красивій дівчині: «А Вашій мамі зять не потрібен?», може, колись і був прикольним, але його час

Сульфат натрію. Розчин сульфату натрію: застосування
Сульфат натрію відноситься до натуральних сольових проносних засобів. М'яко очищає кишечник по всій довжині. Виводить жовч. Є антитоксичним

Сульфат калію - особливості застосування
Для успішного вирощування квітів, садових і городніх рослин необхідно використовувати добрива. Для цього потрібно знати область та особливості