Закон Авогадро: опис і біографія вченого
Передбачити результати дослідження, передбачити закономірність, відчути загальні витоки – всім цим відзначено творчість великого числа експериментаторів та вчених. Найчастіше прогноз поширюється лише на область зайнятості дослідника. І мало в кого вистачає сміливості зайнятися довгостроковими прогнозуванням, істотно випередивши час. У італійця Амедео Авогадро сміливості було хоч відбавляй. Саме з цієї причини цей учений відомий зараз у всьому світі. А закон Авогадро і донині використовується всіма хіміками і фізиками планети. У цій статті ми докладно розповімо про нього і його автора.
У 1803 і 1804 роках Авогадро разом з братом Феліче представив ученим з Туринської Академії дві роботи, що розкривають теорії електрохімічних і електричних явищ. У 1804 році Амедео став членом-кореспондентом цієї академії. У 1806 році Авогадро влаштувався репетитором у Туринський ліцей. А через три роки вчений перебрався в ліцей Верчелли, де викладав математику і фізику протягом десяти років. У той період Амедео прочитав багато наукової літератури, роблячи з книг корисні виписки. Він вів їх до кінця життя. Накопичилося цілих 75 томів по 700 сторінок кожен. Зміст цих книг говорить про різнобічності інтересів вченого і про той колосальний труд, який він зробив.
Дитинство і навчання
Амедео Авогадро народився в Туріні в 1776 році. Його батько Філіпа працював службовцем у судовому відомстві. Усього в родині було восьмеро дітей. Всі предки Амедео служили адвокатами при католицької церкви. Молодий чоловік також не відступив від традиції і зайнявся юриспруденцією. До двадцяти років він вже мав ступінь доктора. З часом юридична практика перестала захоплювати Амедео. Інтереси молодої людини лежали в іншій сфері. Ще в юності він відвідував школу експериментальної фізики та геометрії. Тоді в майбутньому вченому і прокинулася любов до наук. Із-за прогалин у знаннях Авогадро зайнявся самоосвітою. У 25 років Амедео всі вільний час приділяв вивченню математики і фізики.
Наукова діяльність
На першому етапі наукова діяльність Амедео була присвячена вивченню електричних явищ. Інтерес Авогадро особливо посилився після того як Вольт відкрив джерело електричного струму в 1800 році. Не менш цікаві молодому вченому були дискусії Вольта і Гальвані про природу електрики. Та й в цілому тоді ця область була передовою в науці.У 1803 і 1804 роках Авогадро разом з братом Феліче представив ученим з Туринської Академії дві роботи, що розкривають теорії електрохімічних і електричних явищ. У 1804 році Амедео став членом-кореспондентом цієї академії. У 1806 році Авогадро влаштувався репетитором у Туринський ліцей. А через три роки вчений перебрався в ліцей Верчелли, де викладав математику і фізику протягом десяти років. У той період Амедео прочитав багато наукової літератури, роблячи з книг корисні виписки. Він вів їх до кінця життя. Накопичилося цілих 75 томів по 700 сторінок кожен. Зміст цих книг говорить про різнобічності інтересів вченого і про той колосальний труд, який він зробив.
Особисте життя
Сімейне життя Амедео влаштував досить пізно, коли його вік уже перевалив за третій десяток. Працюючи в Верчелли, він зустрів Ганну ді Джузеппе, яка була набагато молодше вченого. У цьому шлюбі народилося вісім дітей. Ніхто з них не пішов по стопах батька.Закон Авогадро та його наслідки
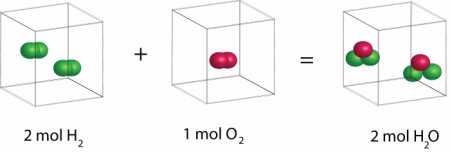
У 1808 році Гей-Люссак (у співавторстві з Гумбольдтом) сформулював принцип об'ємних відносин. Цей закон свідчив, що співвідношення між об'ємами реагуючих газів можна висловити простими числами. Наприклад, 1 об'єм хлору, з'єднуючись з 1 об'ємом водню, дає 2 обсягу хлороводню і т. п. Але цей закон нічого не давав, так як, по-перше, не було конкретного відмінності між поняттями корпускула, молекула, атом, а по-друге, у вчених були різні думки щодо складу частинок різних газів. В 1811 році Амедео зайнявся ретельним аналізом результатів досліджень Гей-Люссака. У підсумку Авогадро зрозумів, що закон об'ємних відносин дозволяє зрозуміти будову молекули газів. Гіпотеза, яку він сформулював, свідчила: «Число молекул будь-якого газу в одному і тому ж обсязі завжди однаково».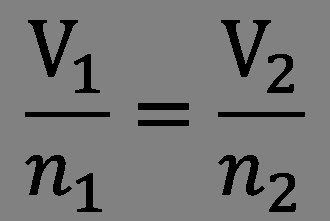
Відкриття закону
Цілих три роки вчений продовжував експериментувати. І в результаті з'явився закон Авогадро, який звучить так: «Рівні обсяги газоподібних речовин при однаковій температурі і тиск містять однакову кількість молекул. А міру маси молекул можна визначити за густини різних газів». Наприклад, якщо 1 літр кисню містить стільки ж молекул, скільки і 1 літр водню, то відношення густин даних газів дорівнює відношенню маси молекул. Також вчений зазначив, що молекули в газах не завжди складаються з одиничних атомів. Допустима наявність як різних, так і однакових атомів. На жаль, у часи Авогадро цей закон не можна було довести теоретично. Але він давав можливість встановлювати в експериментах складу молекул газів і визначати їх масу. Давайте простежимо логіку таких міркувань. У ході експерименту було виявлено, що пари води з газу, а також обсяги водню і кисню співвідносяться в пропорції 2:1:2. З цього факту можна зробити різні висновки. Перший: молекула води складається з трьох атомів, а молекули водню і кисню з двох. Цілком доречний і другий висновок: молекули води і кисню двухатомни, а водню – одноатомни.Противники гіпотези
У закону Авогадро було багато супротивників. Частково це було пов'язано з тим, що в ті часи була відсутня проста і ясна запис рівнянь і формул хімічних реакцій. Головним недоброзичливцем був Йенс Берцеліус – шведський хімік, має незаперечний авторитет. Він вважав, що у всіх атомів є електричні заряди, а самі молекули складаються з атомів з протилежними зарядами, які притягуються один до одного. Так, у атомів водню був позитивний заряд, а у атомів кисню – негативний. З цієї точки зору молекули кисню, що складається з 2-х однаково заряджених атомів, просто не існує. Але якщо молекули кисню все ж одноатомни, то в реакції азоту з киснем пропорція співвідношення обсягів повинна бути 1:1:1. Дане твердження суперечить експерименту, де з 1 літра кисню і 1 літра азоту отримували 2 літри оксиду азоту. Саме з цієї причини Берцеліус і інші хіміки відкидали закон Авогадро. Адже він абсолютно не відповідав експериментальними даними.Відродження закону
До шістдесятих років дев'ятнадцятого століття в хімії спостерігався свавілля. Причому він поширювався як на оцінку молекулярних мас, так і на опис хімічних реакцій. Про атомному складі складних речовин було взагалі багато невірних уявлень. Деякі вчені навіть планували відмовитися від молекулярної теорії. І тільки в 1858 році хімік з Італії по імені Канніццаро знайшов у листуванні Бертолле і Ампера посилання на закон Авогадро та наслідки з нього. Це упорядкувало заплутану картину хімії того часу. Два роки потому Канніццаро розповів про закон Авогадро в Карлсруе на Міжнародному конгресі з хімії. Його доповідь справив незабутнє враження на вчених. Один з них сказав, що він ніби прозрів, всі сумніви зникли, а натомість з'явилося відчуття впевненості. Після того як закон Авогадро визнали, вчені могли не тільки визначати склад молекул газів, але і розраховувати атомні і молекулярні маси. Ці знання допомагали в розрахунку масових співвідношень реагентів у різноманітних хімічних реакціях. І це було дуже зручно. Вимірюючи масу в грамах, дослідники могли оперувати молекулами.Висновок
Багато часу пройшло з тих пір, як був відкритий закон Авогадро, але про основоположнике молекулярної теорії ніхто не забув. Логіка вченого була бездоганною, що пізніше підтвердили розрахунки Дж. Максвелла, засновані на кінетичної теорії газів, а потім і експериментальні дослідження (броунівський рух). Також було визначено, скільки міститься частинок у молі кожного газу. Ця константа – 6022•1023 була названа числом Авогадро, увічнивши ім'я проникливого Амедео.Схожі добрі поради по темі

Ідеальний газ. Рівняння стану ідеального газу. Ізопроцеси.
Ідеальний газ, рівняння стану ідеального газу, його температура і тиск, об'єм список параметрів і ухвал, якими оперують у відповідному розділі

Промислова риба - горбуша. Як відрізнити самку від самця
Смачна і корисна риба живе в Тихому океані - горбуша. Як відрізнити самку від самця - цікавить багатьох покупців. Хтось любить жирних самців, хто

Амедео Авогадро – засновник молекулярної теорії
Амедео Авогадро – відомий італійський фізик і хімік. Є засновником молекулярної теорії. Визнання отримав лише через півстоліття після своєї смерті. У
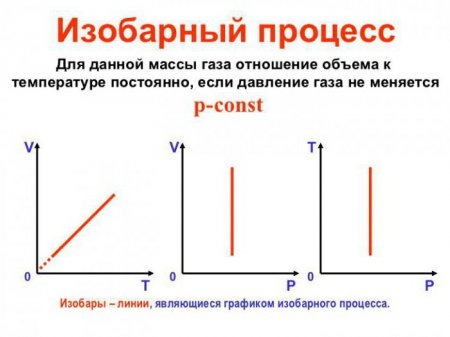
Ізобарний процес, пов'язані з ним рівняння і виведення формули роботи
Ізобарний процес (також званий изобарическим процесом) є однією з термодинамічних процесів, які відбуваються при постійному показнику тиску. Маса

Який камінь підходить Стрільцям-жінкам згідно гороскопу
Зазвичай жінка-Стрілець вибирає собі ті камені, які допомагають їй досягти поставленої мети. Варто зазначити, що вибирати, який камінь підходить
Що таке число Авогадро?
Авогадро - італійський вчений, завдяки якому теорія газів збагатилася кількома дуже цінними гіпотезами. Число Авогадро - одне з таких досягнень,