Склад і будова атомного ядра (коротко)
Задовго до появи достовірних даних про внутрішній устрій всього сущого грецькі мислителі уявляли собі матерію у вигляді дрібних вогняних частинок, які перебували у постійному русі. Ймовірно, це бачення світового устрою речей було виведено з чисто логічних умовиводів. Незважаючи на деяку наївність і абсолютну бездоказовість цього твердження, воно виявилося вірним. Хоча підтвердити сміливу гіпотезу вчені змогли лише двадцять три століття потому.
Катодні промені, які утворювалися поблизу електродів, з'єднаних з негативним кінцем батареї. Катодні промені проходили через трубку і змогли проскочити через отвір в позитивному електроді, як потік заряджених частинок. Спостереження показали, що відношення заряду такої частинки до її маси завжди однаковий і не залежить від виду газу. Позитивні промені. Другий потік частинок йде в протилежному напрямку і може проходити в отвір в негативному електроді. Відхилення в полях доводять, що вони мають високі швидкості і різні значення відношення заряду до маси. Негативні частинки катодних променів були названі електронами. Надалі частинки з тим же відношенням заряду до маси були виявлені в багатьох процесах. Електрони здавалися універсальними складовими різних атомів, досить легко відокремлюються при бомбардуванні іонів і атомів.
Частинки, що несуть позитивний заряд, представлялися осколками атомів після втрати ними одного або декількох електронів. Насправді позитивні промені являли собою групи атомів, позбавлених негативних частинок, і внаслідок цього мають позитивний заряд.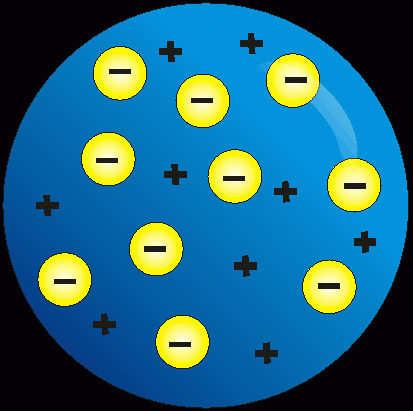
 Відхилення при ударах він пояснює тим, що частинки атома мають власні електричні заряди. Під впливом бомбардують заряджених частинок атомні елементи поводяться як звичайні заряджені тіла в макросвіті: частинки з однаковими зарядами відштовхуються один від одного, а з протилежними – притягуються.
Відхилення при ударах він пояснює тим, що частинки атома мають власні електричні заряди. Під впливом бомбардують заряджених частинок атомні елементи поводяться як звичайні заряджені тіла в макросвіті: частинки з однаковими зарядами відштовхуються один від одного, а з протилежними – притягуються.  Вчений використовував у своїх дослідах метод сцинтиляції – спалаху. За частотою спалахів він робив висновки про те, яким є склад і будову атомного ядра, про характеристики народжених частинок, про їх атомної маси і порядковому номері. Невідома частка була названа Резерфордом протоном. Вона мала всі характеристики атома водню, позбавленого свого єдиного електрона – одиничний позитивний заряд і відповідну масу. Таким чином було доведено, що протон і ядро водню є одними і тими ж частинками. В 1930 році, коли були побудовані і запущені перші великі прискорювачі, модель атома Резерфорда вдалося перевірити і довести: кожен атом водню складається з самотнього електрона, положення якого неможливо визначити, і пухкого атома з одиноким позитивним протоном всередині. Оскільки при бомбардуванні з атома можуть влітати протони, електрони і альфа-частинки, вчені думали, що вони і є складові будь-якого ядра атома. Але подібна модель атома ядра здавалася нестійкою – електрони були занадто великі для того, щоб уміщатися в ядрі, крім цього, існували серйозні труднощі, пов'язані з порушенням закону кількості руху та збереження енергії. Ці два закони, як суворі бухгалтери, говорили про те, що кількість руху і маса при бомбардуванні зникають у невідомому напрямку. Оскільки ці закони були загальноприйнятими, слід було відшукати пояснення для подібної витоку.
Вчений використовував у своїх дослідах метод сцинтиляції – спалаху. За частотою спалахів він робив висновки про те, яким є склад і будову атомного ядра, про характеристики народжених частинок, про їх атомної маси і порядковому номері. Невідома частка була названа Резерфордом протоном. Вона мала всі характеристики атома водню, позбавленого свого єдиного електрона – одиничний позитивний заряд і відповідну масу. Таким чином було доведено, що протон і ядро водню є одними і тими ж частинками. В 1930 році, коли були побудовані і запущені перші великі прискорювачі, модель атома Резерфорда вдалося перевірити і довести: кожен атом водню складається з самотнього електрона, положення якого неможливо визначити, і пухкого атома з одиноким позитивним протоном всередині. Оскільки при бомбардуванні з атома можуть влітати протони, електрони і альфа-частинки, вчені думали, що вони і є складові будь-якого ядра атома. Але подібна модель атома ядра здавалася нестійкою – електрони були занадто великі для того, щоб уміщатися в ядрі, крім цього, існували серйозні труднощі, пов'язані з порушенням закону кількості руху та збереження енергії. Ці два закони, як суворі бухгалтери, говорили про те, що кількість руху і маса при бомбардуванні зникають у невідомому напрямку. Оскільки ці закони були загальноприйнятими, слід було відшукати пояснення для подібної витоку. 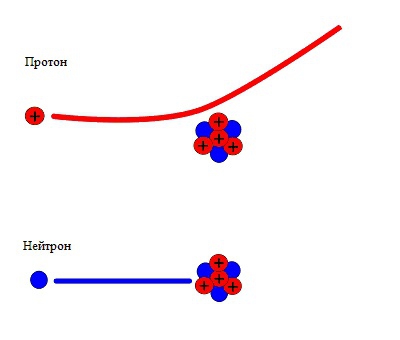
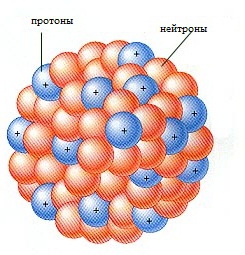 Така картина будови ядра підтверджується експериментами на сучасних великих прискорювачах з швидкими протонами. Електричні сили відштовхування протонів врівноважуються ядреними силами, які діють тільки в самому ядрі. Хоча природа ядерних сил ще до кінця не вивчена, їх існування є практично доведеним і повністю пояснює будову атомного ядра.
Така картина будови ядра підтверджується експериментами на сучасних великих прискорювачах з швидкими протонами. Електричні сили відштовхування протонів врівноважуються ядреними силами, які діють тільки в самому ядрі. Хоча природа ядерних сил ще до кінця не вивчена, їх існування є практично доведеним і повністю пояснює будову атомного ядра.
Будова атомів
В кінці XIX століття були досліджені властивості розрядної трубки, через яку пропущений струм. Спостереження показали, що при цьому випускається два потоку частинок:Частинки, що несуть позитивний заряд, представлялися осколками атомів після втрати ними одного або декількох електронів. Насправді позитивні промені являли собою групи атомів, позбавлених негативних частинок, і внаслідок цього мають позитивний заряд.
Модель Томпсона
На підставі дослідів було з'ясовано, що позитивні і негативні частинки представляли суть атома, були його складовими. Англійський вчений Дж. Томсон запропонував свою теорію. На його думку, будова атома і атомного ядра представляли собою якусь масу, в якій негативні заряди були втиснуті в позитивно заряджений шар, як родзинки в кекс. Компенсація зарядів робила «кекс» електрично нейтральним.
Модель Резерфорда
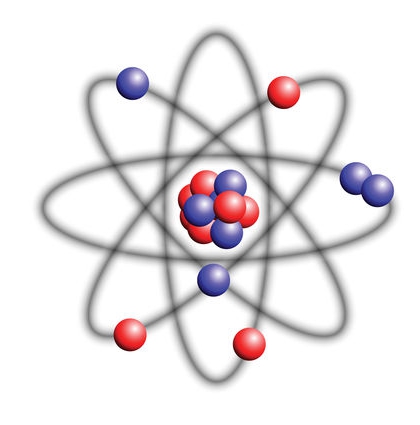
Молодий американський вчений Резерфорд, аналізуючи треки, що залишилися після альфа-частинок, прийшов до висновку, що модель Томпсона недосконала. Деякі альфа-частинки відхилялись на невеликі кути – в 5-10 o . У рідкісних випадках альфа-частинки відхилялися на великі кути в 60-80 o , а у виняткових випадках кути були дуже великими - 120-150 o . Модель атома Томпсона не могла пояснити таку різницю. Резерфорд пропонує нову модель, що пояснює будову атома і атомного ядра. Фізика процесів стверджує, що атом має бути порожнім на 99%, з маленьким ядром і обертаються навколо нього електронами, які рухаються по орбітах.
Стан атомів
На початку минулого століття, коли були запущені перші прискорювачі елементарних частинок, всі теорії, які пояснювали будову атомного ядра і самого атома, чекали експериментальної перевірки. До того часу були вже досконально вивчені взаємодії альфа - і бета-променів з атомами. Аж до 1917 року вважалося, що атоми або стабільні, або радіоактивні. Стабільні атоми не можна розщепити, розпад радіоактивних ядер неможливо контролювати. Але Резерфорду вдалося спростувати цю думку.Перший протон
У 1911 році Е. Резерфорд висунув ідею про те, що всі ядра складаються з однакових елементів, основою для яких є атом водню. На цю ідею вченого наштовхнув важливий висновок попередніх вивчень будови речовини: маси всіх хімічних елементів діляться без залишку на масу водню. Нове припущення відкривало небачені можливості, що дозволяють по-новому бачити будову атомного ядра. Ядерні реакції повинні були підтвердити або спростувати нову гіпотезу. Досліди проводилися в 1919 році з атомами азоту. Бомбардуючи їх альфа-частинками, Резерфорд домігся дивного результату. Атом N поглинув альфа-частинку, перетворився після цього в атом кисню Про 17 і випустив ядро водню. Це стало першим штучним перетворенням атоми одного елемента в інший. Подібний досвід вселяв надію на те, що будова атомного ядра, фізика існуючих процесів дозволяють здійснювати і інші ядерні перетворення.
Нейтрони
Вчені всього світу ставили експерименти, спрямовані на відкриття нових складових ядер атомів. У 1930-х роках німецькі фізики Беккер і Боте бомбардували атоми берилію альфа-частинками. При цьому було зареєстровано невідоме випромінювання, яке було вирішено назвати G-променями. Детальні дослідження розповіли про деякі особливості нових променів: вони могла поширюватися строго по прямій, не взаємодіяли з електричними і магнітними полями, володіли високою проникаючою здатністю. Пізніше частинки, що утворюють цей вид випромінювання, були знайдені при взаємодії альфа-частинок з іншими елементами – бором, хромом та іншими.Гіпотеза Чедвіка
Тоді Джеймс Чедвік, колега і учень Резерфорда, в журналі «Nature» дав коротке повідомлення, яке пізніше стало загальновідомим. Чедвік звернув увагу на той факт, що протиріччя в законах збереження легко вирішуються, якщо допустити, що нове випромінювання є потоком нейтральних частинок, кожна з яких має масу, приблизно рівну масі протона. Розглядаючи це припущення, фізики істотно доповнили гіпотезу, що пояснює будову атомного ядра. Коротко суть доповнень зводилася до нової частинки та її роль у будові атома.
Властивості нейтрона
Виявленої частці було дано ім'я «нейтрон». Нововідкриті частинки не утворювали навколо себе електромагнітних полів, легко проходили через речовину, не втрачаючи при цьому енергії. При рідкісних зіткненнях з легкими ядрами атомів нейтрон в стані вибити з ядро атома, втрачаючи при цьому значну частину своєї енергії. Будова атомного ядра передбачало наявність різної кількості нейтронів в кожному речовині. Атоми з однаковим зарядом ядра, але з різною кількістю нейтронів отримали назву ізотопів. Нейтрони послужили відмінною заміною альфа-частинкам. В даний час саме їх використовують для того, щоб вивчити будову атомного ядра. Коротко їх значення для науки описати неможливо, але саме завдяки бомбардуванню нейтронами атомних ядер фізики змогли отримати ізотопи практично всіх відомих елементів.Склад ядра атома
В даний час будову атомного ядра являє собою сукупність протонів і нейтронів, скріплених між собою ядерними силами. Наприклад, ядро гелію являє собою грудочку з двох нейтронів і двох протонів. Легкі елементи мають практично однакову кількість протонів і нейтронів, у важких елементів кількість нейтронів значно більше.
Зв'язок маси і енергії
У 1932 камера Вільсона зафіксувала дивовижний фотознімок, що доводить існування позитивних заряджених частинок, з масою електрона. До цього позитивні електрони були передбачені теоретично П. Діраком. Реальний позитивний електрон був виявлений також в космічному випромінюванні. Нову частинку назвали позитронів. При зіткненні зі своїм двійником - електроном, відбувається анігіляція – взаємне знищення двох частинок. При цьому звільняється певна кількість енергії. Таким чином, теорія, розроблена для макросвіту, повністю підходила для опису поведінки найдрібніших елементів речовини.Схожі добрі поради по темі
Що таке нейтрон у фізиці: будова, властивості і використання
Що таке нейтрон у фізиці. Його строние, а також важлива роль в стабільності атомного ядра. Історія відкриття нейтрона. Властивості швидких і
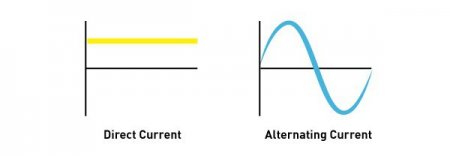
Чим постійний струм відрізняється від змінного і як перетворюється?
Постійний електричний струм — це рух частинок з зарядом у певному напрямку. Тобто його напруга або сила (характеризують величини) мають одне і те ж

Молдова: столиця, найбільші міста і особливості державного устрою республіки
У південно-східній Європі знаходиться маленька країна - сонячна Молдова. Столиця цієї держави - місто Кишинів. Які особливості державного устрою
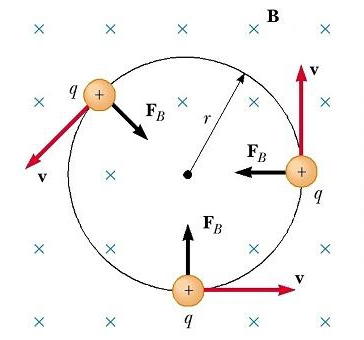
Рух зарядженої частинки в магнітному полі: формули. Рух заряджених частинок в однорідному магнітному полі
Як відомо, електричне поле прийнято характеризувати величиною сили, з якою воно діє на пробний одиничний електричний заряд. Магнітне поле традиційно

Планетарна модель атома: дослід Резерфорда
Планетарну модель атома запропонував Е. Резерфорд в 1910 році. Перші дослідження структури атома були зроблені ним за допомогою альфа-частинок. На

Що таке маса електрона?
Відомо, що електрони мають негативний заряд. Але яким чином можна переконатися в тому, що маса електрона і його заряд постійні для всіх цих частинок?


