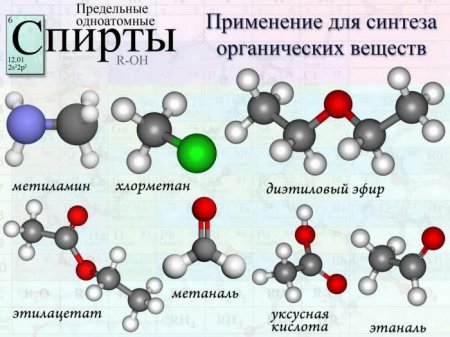
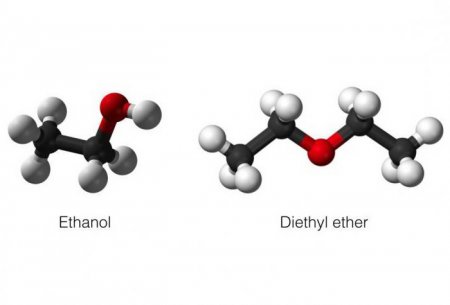
Кисневмісні органічні сполуки, одними з яких є різні спирти, є важливими функціональними похідними вуглеводнів. Вони бувають одноатомними, двох - і багатоатомними. Одноатомні спирти - це, по суті, похідні вуглеводнів, молекулярної складовою яких - одна гидроксильная група (позначається «-OH»), пов'язана з насичені атомами вуглецю.
Поширення
Одноатомні спирти досить широко поширені в природі. Так, метиловий спирт у невеликих кількостях міститься в соку деяких рослин (наприклад, борщівник). Етиловий спирт, будучи продуктом спиртового бродіння органічних сполук, що міститься в подкисших фруктах і ягодах. Цетиловий спирт знайдений в китовому жирі. Бджолиний віск включає церіловий, міріціловий спирти. В пелюстках троянд виявлено 2-фенилэтанол. Терпенові спирти у вигляді запашних речовин представлені в багатьох пряно-ароматичних культур.
Класифікація
Спирти поділяють на молекулярному числа гідроксильних груп. Насамперед на:
одноатомні спирти (наприклад, етанол); двоатомні (этандиол); багатоатомні (гліцерин). По природі вуглеводневого радикала спирти поділяються на ароматичні, аліфатичні, циклічні. В залежності від типу атома вуглецю, що має зв'язок з гідроксильної групою, спирти розглядають як первинні, вторинні і третинні. Загальна формула одноатомного спирту в застосуванні до граничних одноатомним спиртів виражається значенням: З n H 2n + 2 O.
Номенклатура
Назва спиртів по радикально-функціональній номенклатурі утворюється з назви, асоційованого з гідроксильної групою радикала, і слова «спирт». За систематичною номенклатурою IUPAC назва спирту утворюється від відповідного алкана з додаванням закінчення-ол». Наприклад:
метанол – метиловий спирт; метілпропанол-1-2 – ізобутіловий (третбутіловий); етанол – етиловий; бутанол-1-2 – бутиловий (вторбутиловий); пропанол-1-2 – пропіловий (изопрапиловий). Нумерація за правилами IUPAC класифікується положенням гідроксильної групи, вона отримує менший номер. Наприклад: пентандиол-2-4 4-метилпентанол-2 і т. д.
Ізомерія
Граничні одноатомні спирти володіють наступними типами структурної і просторової ізомерії. Наприклад:
Вуглецевого скелета. Ізомерні простих ефірів. Положення функціональної групи. Просторова ізомерія спиртів представлена оптичною ізомерією. Оптична ізомерія можлива при наявності в молекулі асиметричного атома вуглецю (містить чотири різних заступника).
Способи отримання одноатомних спиртів
Отримати граничний одноатомний спирт можна декількома методами:
Гідролізом галогеналканов. Гідратацією алкенів. Відновлення альдегідів і кетонів. Магнийорганическим синтезом. Гідроліз галогеналканов – це один з поширених лабораторних способів отримання спиртів. Обробкою водою (як альтернатива – водним розчином лугу) спирти отримують первинні і вторинні: CH 3 - CH 2 -Br + NaOH -> CH 3 - CH 2 - OH + NaBr. Третинні галогеноалкани гідролізуються ще легше, однак у них легше протікає побічна реакція елімінування. Тому третинні спирти отримують іншими методами. Гідратація алкенів здійснюється приєднанням до алкенам води в присутності кислотовмісних каталізаторів (H 3 PO 4) . Метод лежить в основі промислового отримання таких спиртів, як етиловий, ізопропіловий, трет-бутиловий. Відновлення карбонільної групи здійснюють воднем у присутності каталізатора гідрування (Ni або Pt). З кетонів при цьому утворюються вторинні спирти, альдегіди – первинні граничні одноатомні спирти. Формула процесу: CH 3 - C = O (H) + H 2 (этаналь) -> CH 3 - CH 2 - OH (етанол). Приєднанням до альдегідів і кетонам алкилмагнийгалогенидов одержують магній-органічні сполуки. Реакцію проводять в сухому діетиловому ефірі. Подальший гідроліз магнійорганіческіх сполук утворює одноатомні спирти. Первинні спирти утворюються за реакцією Гриньяра тільки з формальдегіду та будь-яких алкилмагнийгалогенидов. Інші альдегіди дають по цій реакції вторинні спирти, кетони – третинні спирти.
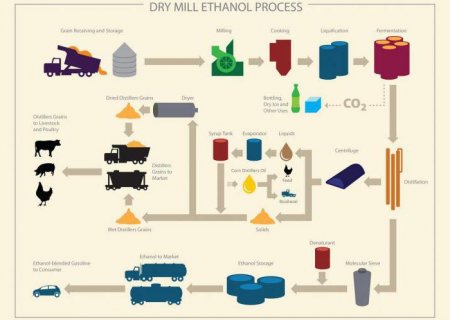
Промисловий синтез метанолу
Промислові методи, як правило, є безперервними процесами з багаторазовою рециркуляцією великих мас реагуючих речовин, що здійснюються в газовій фазі. Промислово важливими спиртами є метанол і етанол. Метанол (його обсяги виробництва найбільші серед спиртів) до 1923 року отримували сухий перегонкою (нагріванням без доступу повітря) деревини. Сьогодні його генерують із синтез-газу (суміші CO і H 2 ). Процес проводять під тиском 5-10 МПа з використанням оксидних каталізаторів (ZnO + Cr 2 O 3 , CuO + ZnO + Al 2 O 3 та інших) в інтервалі температур 250-400С, в результаті отримували граничні одноатомні спирти. Формула реакції: CO + 2H 2 -> CH 3 OH. У 80-ті роки при вивченні механізму цього процесу було встановлено, що метанол утворюється не з чадного газу, а з вуглекислого газу, получающегося при взаємодії чадного газу зі слідами води.
Промисловий синтез етанолу
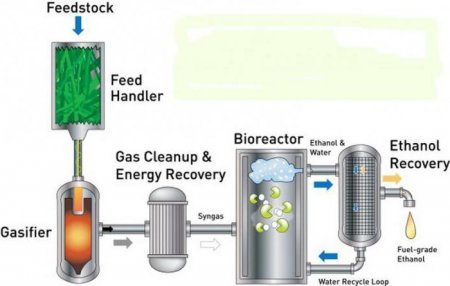
Поширеним виробничим методом синтезу технічного етанолу є гідратація етилену. Формула одноатомного спирту етанолу отримає наступний вигляд: CH 2 = CH 2 + H 2 O -> CH 3 - CH 2 OH. Процес проводять під тиском 6-7 МПа в газовій фазі, пропускаючи етилен і пари води над каталізатором. Каталізатором виступають фосфорна або сірчана кислоти, нанесені на силікагель. Харчової та медичний етиловий спирт отримують ферментативним гідролізом цукрів, що містяться у винограді, ягодах, злаках, картоплі з подальшим зброджуванням утворюється глюкози. Бродіння цукристих речовин викликається дріжджовими грибками, що відносяться до групи ферментів. Для процесу найбільш сприятлива температура 25-30С. На промпідприємствах застосовують етанол, отриманий зброджуванням утворюються при гідролізі деревини та відходів целюлозно-паперового виробництва вуглеводів.
Фізичні властивості одноатомних спиртів
У молекулах спиртів існують атоми водню, пов'язані з електронегативний елемент – киснем, практично позбавлені електронів. Між цими атомами водню і атомами кисню, що мають неподеленние пари електронів, що утворюються міжмолекулярні водневі зв'язки. Воднева зв'язок обумовлена специфічними особливостями атома водню:
При відтягуванні зв'язуючих електронів до більш электроотрицательному атому ядро атома водню «оголюється», і утворюється неекранований іншими електронами протон. При іонізації будь-якого іншого атома все одно залишається електронна оболонка, екрануюча ядро. Атом водню має малий розмір у порівнянні з іншими атомами, внаслідок чого він здатний досить глибоко впроваджуватися в електронну оболонку сусіднього негативно поляризованого атома, не з'єднуючись з ним ковалентним зв'язком. Воднева зв'язок приблизно в 10 разів слабкіше звичайної ковалентного. Енергія водневого зв'язку знаходиться в межах 4-60 кДж/моль, для молекул спиртів вона становить 25 кДж/моль. Від звичайних s-зв'язків вона відрізняється більшою довжиною (0166 нм) порівняно з довжиною зв'язку O-H (0107 нм).
Хімічні властивості
Хімічні реакції одноатомних спиртів визначаються наявністю в їх молекулах гідроксильної групи, яка є функціональною. Атом кисню знаходиться в sp3-гібридному стані. Валентний кут близький до тетраэдрическому. Дві sp3-гібридні орбіталі йдуть на утворення зв'язків з іншими атомами, а на двох інших осях знаходяться неподеленние пари електронів. Відповідно, на атомі кисню зосереджений частковий негативний заряд, а на атомах водню і вуглецю – часткові позитивні заряди. Зв'язку C-O і C-H – ковалентні полярні (остання більш полярна). Гетеролитический розрив зв'язку O-H з утворенням H+ обумовлює кислотні властивості одноатомних спиртів. Атом вуглецю з частковим позитивним зарядом може бути об'єктом атаки нуклеофільного реагенту.
Кислотні властивості
Спирти є дуже слабкими кислотами, більш слабкими, ніж вода, але більш сильними, ніж ацетилен. Вони не викликають зміни забарвлення індикатора. Окислення одноатомних спиртів проявляється при взаємодії з активними металами (лужними і лужно-земельними) з виділенням водню і утворенням алкоголятов: 2ROH + 2Na -> 2RONa + H 2. Алкоголяти лужних металів – речовини з іонним зв'язком між киснем і натрієм, в розчині одноатомного спирту вони дисоціюють з утворенням алкосид-іонів: CH 3 Vona -> CH 3 O - + Na + (метоксид-іон). Освіта алкоголятов можливо також здійснити по реакції спирту з аміда натрію: C 2 H 5 OH + NaNH 2 -> C 2 H 5 ONa + NH 3 . А чи відбудеться реакція етанолу з лугом? Практично немає. Вода – більш сильна кислота, ніж етиловий спирт, тому тут встановлюється рівновага. Із збільшенням довжини вуглеводневого радикалу в молекулі спирту кислотні властивості знижуються. Також граничні одноатомні спирти характеризуються зниженням кислотності в ряду: первинний -> вторинний -> третинний.
Реакція нуклеофільного заміщення
В спиртах зв'язок C-O поляризована, на атомі вуглецю зосереджений частковий позитивний заряд. Як наслідок – атом вуглецю атакується нуклеофільними частинками. В процесі розриву зв'язку C-O відбувається заміщення іншим нуклеофилом гідроксильної групи. Однією з таких реакцій є взаємодія спиртів з галогенводородами або їх концентрованими розчинами. Рівняння реакції: C 2 H 5 OH + HBr -> C 2 H 5 Br + H 2 O. Для полегшення відщеплення гідроксильної групи використовують в якості каталізатора концентровану сірчану кислоту. Вона протонирует атом кисню, тим самим активуючи молекулу одноатомного спирту. Первинні спирти, як і первинні галогеноалкани, вступають у реакції обміну з механізмом SN 2 . Вторинні одноатомні спирти, як і вторинні галогеноалкани, реагують з галогеноводородними кислотами. Умови взаємодії спиртів підпорядковані природи реагуючих компонентів. Реакційна здатність спиртів підпорядковується наступній закономірності: R 3 COH -> R 2 CHOH -> RCH 2 OH.
Окислення
У м'яких умовах (нейтральні або лужні розчини перманганату калію, хромової суміші при температурі 40-50°С) окислюються первинні спирти до альдегідів, при нагріванні до більш високої температури – до кислот. Вторинні спирти проходять процес окислення до кетонів. Третинні окислюються в присутності кислоти у дуже жорстких умовах (наприклад, хромовою сумішшю при температурі 180°С). Реакція окислення третинних спиртів йде через дегідратації спирту з утворенням алкена і окисленням останнього з розривом подвійний зв'язку.