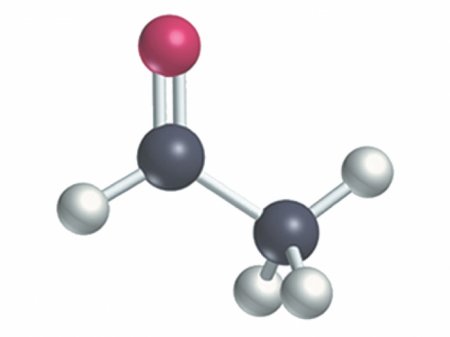
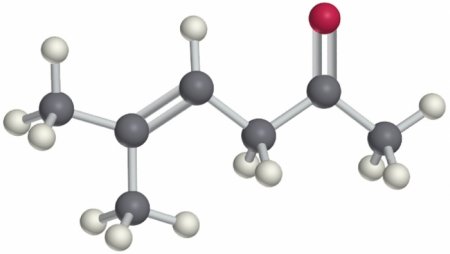
Альдегіди та кетони. Формула, отримання, застосування
Серед кисневмісних органічних сполук величезне значення мають цілих два класи речовин, які завжди вивчають разом за схожість в будові і проявляються властивості. Це альдегіди і кетони. Саме ці молекули лежать в основі багатьох хімічних синтезів, а їх будова досить цікаве, щоб стати предметом вивчення. Розглянемо докладніше, що ж являють собою ці класи сполук.
Кетони також можуть бути граничними і неграничними, так і проявляються властивості схожі з близкородственним класом. Можна навести кілька прикладів, що ілюструють складу молекул і відображають прийняті позначення формул розглянутих речовин. Альдегіди: метаналь - НСОН, бутаналь - СН 3 -СН 2 -СН 2 -СОН, фенилуксусний - З 6 Н 5 -СН 2 -СОН. Кетони: ацетон або диметилкетон - СН 3 -СО-СН 3 , метилетилкетон - СН 3 -З-З 2 Н 5 та інші.
Очевидно, що назва даних сполук утворюється двома шляхами: за раціональною номенклатурою згідно входять до складу радикалам і класового суфікса-аль (для альдегідів)- він (для кетонів); тривіально, історично склалося. Якщо привести загальну формулу для обох класів речовин, то стане видно, що вони є ізомерами один одному: C n H 2n O. Для них же самих характерні такі види ізомерії:
для кетонів - будова вуглеводневої ланцюга радикала і положення групи-З; для альдегідів - тільки розташування атомів у ланцюгу. Щоб розрізняти між собою представників обох класів, використовують якісні реакції, більшість з яких дозволяють виявити саме альдегід. Так як хімічна активність даних речовин декілька вище, завдяки наявності катіонів водню. Атом вуглецю, безпосередньо входить у функціональну групу, має sp 2 - гібридизацію, що дозволяє частини молекули мати плоску просторову форму. При цьому полярність зв'язку З=Про сильна. Як більш електронегативний, кисень забирає собі основну частину щільності, концентруючи на собі частково негативний заряд. У альдегидах зв'язок О-Н є також сильно поляризованою, що робить атом водню рухомим. У результаті виходить, що подібну будову молекул дозволяє досліджуваних сполук і окислюватися, і відновлюватися. Формула альдегіду і кетону з перераспределенной електронною щільністю дозволяє передбачити продукти реакцій, в яких беруть участь ці речовини. Перший представник метаналь за агрегатним станом - газ, наступні одинадцять - рідини, понад 12 атомів вуглецю входять до складу твердих альдегідів нормальної будови. Температура кипіння: залежить від числа атомів З, чим їх більше, тим вона вища. При цьому чим більш розгалужена ланцюжок, тим нижче опускається значення температури. Для рідких альдегідів показники в'язкості, щільності, заломлення залежать також від числа атомів. Чим їх більше, тим вони вищі. Газоподібний і рідкі альдегіди розчиняються у воді дуже добре, проте тверді практично не можуть цього робити. Запах представників дуже приємний, часто це аромати квітів, парфумів, фруктів. Лише ті альдегіди, в яких кількість атомів вуглецю дорівнює 1-5 є сильно і неприємно пахнуть рідинами. Якщо позначати властивості кетонів, то також можна виділити головні. Агрегатні стани: нижчі представники - рідини, більш масивні тверді з'єднання. Запах різкий, неприємний у всіх представників. Розчинність у воді хороша у нижчих, в органічних розчинниках чудова у всіх. Летючі речовини, даний показник перевищує такий в кислот, спиртів. Температура кипіння і плавлення залежить від будови молекули, сильно варіюється від кількості атомів вуглецю в ланцюгу. Це основні властивості даних сполук, які відносяться до групи фізичних. Окислення до відповідних карбонових кислот. Загальний вигляд рівняння реакції: R-COH +[O]= R-COOH. Ароматичні представники ще легше вступають в подібні взаємодії, також вони здатні формувати в результаті складні ефіри, які мають важливе промислове значення. В якості окислювачів використовують: кисень, реактив Толленса, гідроксид міді (II) та інші. Альдегіди проявляють себе як сильні відновники, при цьому перетворюючись в граничні одноатомні спирти. Взаємодія із спиртами, з утворенням продуктів ацеталей і полуацеталей. Особливі реакції поліконденсації. В результаті утворюються фенолформальдегідні смоли, які мають значення для хімічної промисловості. Кілька специфічних реакцій з такими реактивами: водно-спиртова луг; реактив Гриньяра; гидросульфити та інші. Якісною реакцією на даний клас речовин є реакція "срібного дзеркала". В результаті неї утворюється металеве відновлене срібло і відповідна карбонова кислота. Для неї необхідний аміачний розчин оксиду срібла або реактив Толлинса. Окислювальні властивості. В результаті утворюються вторинні спирти. Гідрування також призводить до згаданих вище продуктів. Кето-енольная таутомерія - особливе специфічне властивість кетонів приймати бета-форму. Реакції альдольної конденсації з утворення бета-кетоспиртов. Також кетони здатні взаємодіяти з: аміаком; синильною кислотою; гидросульфитами; гідразином; ортокремнієвої кислоти. Очевидно, що реакції таких взаємодій дуже складні, особливо ті, які є специфічними. Це всі основні особливості, які проявляють альдегіди і кетони. Хімічні властивості лежать в основі багатьох синтезів важливих сполук. Тому знати природу молекул і їх характер при взаємодіях вкрай необхідно в промислових процесах. Синильна кислота, утворюються циангидрини - вихідна сировина при синтезі амінокислот. Аміак, аміни. Спирти. Воду. Гідросульфат натрію. Реактив Гриньяра. Тиоли та інші. Ці реакції мають важливе промислове значення, оскільки продукти використовуються в різних сферах життєдіяльності людей. Найпоширенішим методом, в тому числі і в лабораторіях, є окислення відповідних спиртів: первинних до альдегідів, вторинних до представників кетонів. Як окисного агента можуть виступати: хромати, іони міді, перманганат калію. Загальний вигляд реакції: R-OH + Cu (KMnO 4 ) = R-COH. У промисловості часто використовують спосіб, заснований на окисленні алкенів - оксосинтез. Основний агент синтез-газ, суміш З 2 + Н 2 . Результатом стає альдегід з великим на один вуглець числом атомів у ланцюгу. R=R-R + З 2 + Н 2 = R-R-R-COH. Окиснення алкенів озоном - озонолиз. Результат також передбачає альдегід, але крім цього ще й кетон в суміші. Якщо продукти подумки з'єднати, прибравши кисень, стане ясно, який вихідний алкен був узятий. Реакція Кучерова - гідратація алкіной. Обов'язковий агент - солі ртуті. Один з промислових способів синтезу альдегідів і кетонів. RR-R + Hg 2+ + H 2 O = R-R-COH. Гідроліз дигалогенпроизводних вуглеводнів. Відновлення: карбонових кислот, амідів, нітрилів, хлорангидридов, складних ефірів. В результаті утворюється як альдегід, так і кетонів. Піроліз сумішей карбонових кислот над каталізаторами у вигляді оксидів металів. Суміш повинна бути пароподібний. Суть полягає в отщеплении між молекулами діоксиду вуглецю і води. В результаті утворюється альдегід або кетон. Ароматичні альдегіди і кетони отримують іншими способами, так як дані сполуки мають ароматичний радикал (феніл, наприклад). По Фриделю-Крафтсу: у вихідних реагентах ароматичний вуглеводень і дигалогензамещенний кетон. Каталізатор - ALCL 3 . В результаті утворюється ароматичний альдегід або кетон. Інша назва процесу - ацилювання. Окиснення толуолу дією різних агентів. Відновленням ароматичних карбонових кислот. Природно, що в промисловості намагаються використовувати ті методи, в яких вихідна сировина як можна дешевше, а каталізатори менш токсичні. Для синтезу альдегідів - це окиснення алкенів киснем. фармацевтика; хімічний синтез; медицина; парфумерна область; харчова промисловість; лакофарбове виробництво; синтез пластмас, тканин тощо. Можна позначити ще не одну область, адже щороку тільки формальдегіду синтезується приблизно 6 млн т в рік! Його 40% розчин називається формаліном і використовується для зберігання анатомічних об'єктів. Він же йде на виготовлення лікарських препаратів, антисептиків і полімерів. Оцтовий альдегід, або этаналь, також масово вироблений продукт. Кількість щорічного споживання в світі становить близько 4 млн т. Він - основа багатьох хімічних синтезів, при яких утворюються важливі продукти. Наприклад: оцтова кислота та її ангідрид; ацетат целюлози; ліки; бутадієн - основа каучуку; етиловий спирт; ацетатное волокно. Ароматичні альдегіди і кетони - це складова частина багатьох ароматизаторів, як харчових, так і парфумерних. Більшість з них мають дуже приємні квіткові, цитрусові, трав'яні аромати. Це дозволяє виготовляти на їх основі: освіжувачі повітря різного роду; туалетні та парфумерні води; різні чистячі і миючі засоби. Деякі з них є ароматичними добавками до їжі, дозволеними до вживання. Їх природний вміст в ефірних оліях, фруктах і смолах доводять можливість подібного використання. педіатрія - зниження внутрішньочерепного тиску; нормалізація артеріального тиску у дорослих; компонент ліки для органів зору; складова частина багатьох запашних речовин; протизапальний засіб та антисептик; сировина для синтезу ретинолу; ароматизатор в харчових цілях.
Альдегіди і кетони: загальна характеристика
З точки зору хімії, до класу альдегідів слід вносити органічні молекули, що містять кисень у складі функціональної групи-СОН, званої карбонільної. Загальна формула в цьому випадку буде виглядати так: R-COH. За своєю природою це можуть бути як граничні, так і неграничні з'єднання. Також серед них зустрічаються і ароматичні представники, нарівні з аліфатичними. Кількість атомів вуглецю у радикальної ланцюга варіюється в досить широких межах, від одного (формальдегід або метаналь) до декількох десятків. Кетони також містять карбонильную групу-ЗІ, однак вона не з'єднана з катіоном водню, а з іншим радикалом, відмінним або ідентичним тому, що входить в ланцюг. Загальна формула виглядає так: R-CO-R , . Очевидно, що альдегіди і кетони схожі за наявності функціональної групи такого складу.Кетони також можуть бути граничними і неграничними, так і проявляються властивості схожі з близкородственним класом. Можна навести кілька прикладів, що ілюструють складу молекул і відображають прийняті позначення формул розглянутих речовин.
Будова молекули
Розглянемо, як же в просторі виглядають альдегіди і кетони. Будова їх молекул можна відобразити кількома пунктами.Історія відкриття і вивчення
Як і багато органічні сполуки, виділити і вивчити альдегіди і кетони людям вдалося лише в XIX столітті, коли виталистические погляди повністю обвалилися і стало зрозуміло, що ці сполуки можуть утворюватися синтетичним, штучним шляхом, без участі живих істот. Однак ще в 1661 Р. Бойль зумів отримати ацетон (диметилкетон), коли піддавав нагрівання ацетат кальцію. Але детально вивчити це речовина і назвати його, визначити систематичне положення серед інших, він не зміг. Лише в 1852 році Вільямсон зумів довести цю справу до кінця, тоді й почалася історія докладного розвитку і накопичення знань про карбонільних сполуках.Фізичні властивості
Розглянемо, які фізичні властивості альдегідів і кетонів. Почнемо з перших.Хімічні властивості
Найважливіше, це з чим реагують альдегіди і кетони, хімічні властивості даних сполук. Тому їх ми обов'язково розглянемо. Спочатку розберемося з альдегідами.Хімічні властивості кетонів
Спирти, альдегіди, кетони є схожими за що проявляються властивостями сполуками, так як всі вони кисневмісні. Проте вже на стадії окислення стає ясно, що спирти - найбільш активні і легко піддаються впливу сполуки. Кетони ж окислити найважче.Реакції приєднання альдегідів і кетонів
Ми вже розглянули дані реакції, проте не давали їм такої назви. До приєднання можна віднести всі взаємодії, в результаті яких активність проявила карбонільна група. А точніше, рухливий атом водню. Саме тому в даному питанні перевага віддається саме альдегідів, внаслідок їх кращого реакционноспособности. З якими речовинами можливі реакції альдегідів і кетонів по нуклеофільного заміщення? Це:Способи отримання
Існує кілька основних методів, якими синтезують альдегіди і кетони. Отримання в лабораторії і промисловості можна виразити в таких способах.Застосування в промисловості і значення
Застосування альдегідів і кетонів здійснюється в таких галузях промисловості, як:Окремі представники
Такий альдегід, як цитраль, являє собою рідину з великою в'язкістю і сильним ароматом лимона. У природі міститься якраз в ефірних маслах останнього. Також у складі евкаліпта, сорго, кебаба. Добре відомі області його застосування:Схожі добрі поради по темі
Загальна формула амінів. Властивості та будова амінів
Органічні основи – таку назву часто використовують у хімії для сполук, які є похідними аміаку. Атоми водню в його молекулі заміщені на вуглеводневі

Хімічні властивості алкадієнів - ненасичених вуглеводнів
Відмінною особливістю всіх неграничних вуглеводнів є наявність у їх молекулах пі-зв'язків, званих ще подвійними. Алкадиены являють собою відкриті
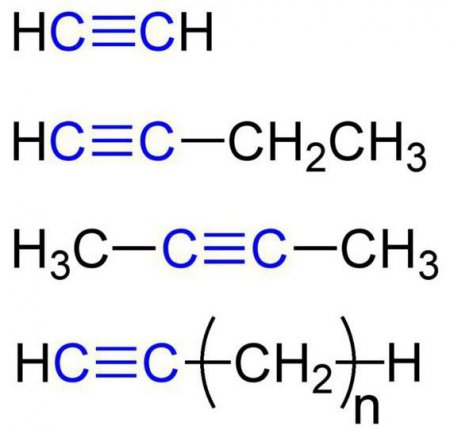
Хімічні властивості алкіной. Будова, отримання, застосування
Що таке алкины? Якими фізичними і хімічними властивостями вони володіють? Де застосовуються? Які існують способи їх отримання?
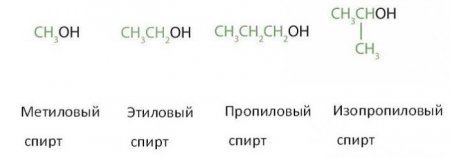
Отримання спиртів, застосування, властивості. Способи одержання спиртів
Спирти поширені в природі. Більшість людей знайомі з етиловим спиртом (етанолом) - активним інгредієнтом алкогольних напоїв, але він є лише одним з

Столиця Колумбії, її визначні пам'ятки і фото
Санта-фе-де-Богота (скорочена назва - Богота) - столиця Колумбії, розташована в самому центрі цієї країни на висоті 2574 м (в межах Східної

Органічні сполуки. Класи органічних сполук
Органічні сполуки є самим численним класом речовин. Тут є близько 20 видів речовин. Вони різні за хімічним властивостям, відрізняються фізичними